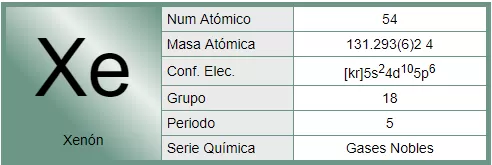
El xenón es un elemento químico de la tabla periódica cuyo símbolo es Xe y su número atómico el 54. Gas noble inodoro, muy pesado, incoloro, el xenón está presente en la atmósfera terrestre solo en trazas y fue parte del primer compuesto de gas noble sintetizado.
El xenón es un miembro de los elementos de valencia ocho llamados gases nobles o inertes. La palabra "inerte" ya no se usa para describir esta serie química, dado que algunos elementos de valencia cero forman compuestos. En un tubo lleno de gas xenón, se emite un brillo azul cuando se le excita con una descarga eléctrica. Se ha conseguido xenón metálico aplicándole presiones de varios cientos de kilobares. El xenón también puede formar clatratos con agua cuando sus átomos quedan atrapados en un entramado de moléculas de oxigeno.
Abundancia
Se encuentra en trazas en la atmósfera terrestre, apareciendo en una parte por veinte millones. El elemento se obtiene comercialmente por extracción de los residuos del aire licuado. Este gas noble se encuentra naturalmente en los gases emitidos por algunos manantiales naturales. Los isótopos Xe-133 y Xe-135 se sintetizan mediante irradiación de neutrones en reactores nucleares refrigerados por aire.
Isótopos
En la naturaleza, el xenón se encuentra en siete isótopos estables y dos ligeramente radioactivos. Además de estas formas estables, se han estudiado 20 isótopos inestables más. El Xe-129 se produce por emisión beta del I-129 (periodo de semidesintegración: 16 millones de años); los isótopos Xe-131, Xe-132, Xe-134 y Xe-136 son productos de fisión tanto del U-238 como del Pu-244. Al ser el xenón un trazador con dos isótopos padres, la medición de los isótopos de xenón en los meteoritos resulta ser una poderosa herramienta para el estudio de la formación del Sistema Solar. El método I-Xe de datación radiométrica permite calcular el tiempo transcurrido entre la nucleosíntesis y la condensación de un objeto sólido a partir de la nebulosa solar. Los isótopos de xenón también son útiles para entender la diferenciación terrestre. Se cree que el exceso de Xe-129 encontrado en emanaciones gaseosas de dióxido de carbono en Nuevo México se debe al decaimiento de gases derivados del manto poco después de la formación de la Tierra.
Aplicaciones
El uso principal y más famoso de este gas es en la fabricación de dispositivos emisores de luz tales como lámparas bactericidas, tubos electrónicos, lámparas estroboscópicas y flashes fotográficos, así como en lámparas usadas para excitar láseres de rubí, que generan de esta forma luz coherente. Otros usos son:
- Como anestésico en anestesia general.
- En instalaciones nucleares, se usa en cámaras de burbujas, sondas, y en otras áreas donde el alto peso molecular es una cualidad deseable.
- Los perxenatos se usan como agentes oxidantes en química analítica.
- El isótopo Xe-133 se usa como radioisótopo.
- Se usa en los faros de automóviles.
- Las lámparas de xenón son ampliamente utilizadas en los proyectores de cine.
- Gas de propulsión iónica para satélites.
- En impresoras o copiadoras para que la tinta selle en la hoja de papel.
Precauciones
El gas puede ser almacenado con seguridad en contenedores convencionales de vidrio sellados a temperatura y presión ambientes. El xenón no es tóxico, pero varios de sus compuestos lo son altamente debido a sus fuertes propiedades de oxidación.
Este gas produce un efecto contrario al Helio y al ser inhalado hace su voz más grave.