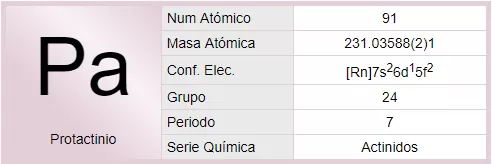
El protactinio es un elemento químico de la tabla periódica cuyo símbolo es Pa y su número atómico es 91, es un elemento metálico plateado que pertenece al grupo de los actínidos, que presenta un brillo metálico intenso. Es superconductor por debajo de 1.4 K.
Abundancia
El protactinio natural se produce por la desintegración radiactiva del uranio y el torio, por tanto se encuentra en todos sus minerales, siendo su concentración proporcional al porcentaje de dichos elementos. En la pechblenda se halla en una cantidad de aproximadamente una parte de 231Pa en 10 millones de mena (es decir, 0,1 ppm). Algunas menas de la República Democrática del Congo llegan a tener en torno a 3 ppm.
Isótopos
Se han caracterizado 29 radioisótopos del protactinio siendo los más estables el 231Pa, con una vida media de 32.760 años; el 233Pa, con una vida media de 26,967 días; y el 230Pa con una vida media de 17,4 días. El resto de isótopos radiactivos tienen vidas medias inferiores a 1,6 días y la mayoría tienen vidas medias menores de 1,8 segundos. Este elemento también tiene dos metaestados, 217mPa (vida media de 1,15 milisegundos) y 234mPa (vida media de 1,17 minutos).
El modo de desintegración primario del isótopo más estable 231Pa y de aquellos más ligeros es la desintegración alfa mientras que para los isótopos más pesados es la desintegración beta. Los productos primarios de la desintegración de los isótopos más ligeros (231Pa o más ligeros) son isótopos del actinio (Ac) mientras que los isótopos más pesados producen isótopos del uranio (U).
Aplicaciones
Debido a su escasez, alta radioactividad y toxicidad, actualmente no existen usos para el protactinio fuera de la investigación científica básica.
Precauciones
El protactinio es tóxico y altamente radiactivo. Por este motivo, requiere precauciones similares a las usadas cuando se maneja plutonio.