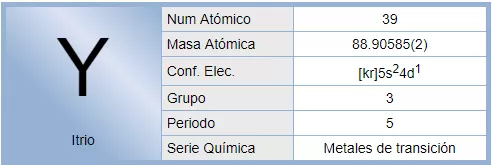
El itrio es un elemento químico de la tabla periódica cuyo símbolo es Y y su número atómico es 39. Su peso atómico es 88,905. Es una tierra rara de transición del grupo IIIB. Es un metal plateado de transición, común en los minerales de tierras raras.
El itrio es un metal plateado, brillante, ligero, dúctil y maleable. Su punto de ebullición es de 3609 K. Químicamente se asemeja a los lantánidos. Es bastante estable en el aire, ya que arde por encima de los 600 K, pero reactivo en ciertas condiciones. El polvo del metal y sus virutas pueden encenderse a temperatura ambiente.
El itrio es la tierra rara más abundante. Incluso llega a ser el doble de abundante que el plomo, pero es difícil de extraer.
Obtención
Los metales raros pueden ser extraídos por medio de disolventes o a partir de métodos de intercambio iónico. El itrio puro comercial se separa de otras tierras raras por medio de intercambio iónico; el metal del itrio se obtiene por reducción del fluoruro con calcio.
Isótopos
El itrio natural se compone de solamente un isótopo (Y-89). Los radioisótopos más estables son Y-88 que tiene un periodo de semidesintegración de 106,65 días y Y-91 con uno de 58,51 días. El resto de isótopos tienen unos periodos de semidesintegración de menos que un día excepto Y-87 que tiene uno de 79,8 horas. Se han catalogado 26 isótopos inestables. El ion Y3+ es diamagnético.
Aplicaciones
- El itrio se utiliza comercialmente en la industria metálica para aleaciones.
- El óxido de itrio se emplea para producir granates de itrio-hierro (Y3Fe5Si3O12), muy eficientes como filtros de microondas y también en la transmisión y transducción de energía acústica.
- El óxido de itrio con aluminio (Y3Al5Si3O12) y gadolinio (Y3Gd5Si3O12) tienen interesantes propiedades magnéticas. El de aluminio tiene una dureza de 8.5 en la escala de Mohs y se usa como piedra preciosa similar al diamante.
- Cantidades pequeñas del elemento (0,1 a 0,2 %) se han utilizado para reducir el tamaño de grano del cromo, del molibdeno, del titanio, y del circonio. También se utiliza para aumentar la fuerza de aleaciones como el aluminio y el magnesio.
- Se usa como catalizador para la polimerización del etileno.
- Se utiliza como “atrapador” para eliminar oxígeno e impurezas de otros materiales; esto le permite reducir el óxido de vanadio y otros metales no ferrosos.
- Utilizado como componente de las pantallas intensificadoras de las unidades de rayos X.
- Añadido en la formulación de las baterías de Li-ion: LiFePO4 pasa a ser LiFeYPO4 aumentando el número de ciclos útiles y mejorando la velocidad de recarga. Estas baterías se utilizan en motocicletas eléctricas.
- El Yttralox es una cerámica transparente hecha a partir de óxido de itrio, la cual tiene un punto de fusión de 2477 K. Es usada en lentes que tienen que resistir altas temperaturas, ventanas infrarrojas, láseres y lámparas de alta intensidad
- El itrio forma la matriz de los fósforos de itrio y europio activados, que emiten una luz brillante y roja clara cuando son excitados por electrones. La industria de la televisión utiliza esos fósforos en la manufactura de pantallas de televisión. Esto se logra añadiendo pequeñas cantidades de europio al vanadato de itrio.
- En pequeñas cantidades se añade óxido de itrio a las superaleaciones de níquel usadas en turbinas de aviación para mantener sus propiedades mecánicas a altas temperaturas.
El uso del itrio está todavía creciendo, debido en realidad a sus buenas condiciones para producir catalizadores y brillo en el cristal.
Precauciones
El itrio es peligroso en el ambiente de trabajo, debido a que las partículas y los gases pueden ser inhalados en el aire. Puede producir daño en los pulmones, especialmente durante exposiciones a largo plazo. El itrio puede también causar cáncer en humanos, así como aumentar las posibilidades de cáncer de pulmón cuando es inhalado. Finalmente, puede ser una amenaza para el hígado cuando se acumula en el cuerpo humano.