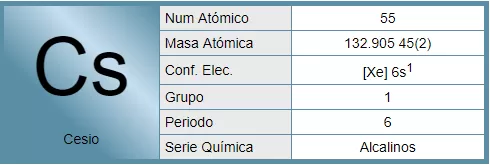
El cesio es el elemento químico con número atómico 55 y peso atómico de 132,905 uma. Su símbolo es Cs, y es el más pesado de los metales alcalinos en el grupo IA de la tabla periódica, a excepción del francio.
El cesio es un metal blando, ligero y de bajo punto de fusión. Es el segundo menos electronegativo de todos los elementos después del francio. El cesio reacciona en forma vigorosa con oxígeno para formar una mezcla de óxidos. En aire húmedo, el calor de oxidación puede ser suficiente para fundir y prender el metal. El cesio no reacciona con nitrógeno para formar nitruros, pero reacciona con el hidrógeno a temperaturas altas para producir un hidruro muy estable; reacciona en forma violenta con el agua y aun con hielo a temperaturas de hasta -116 °C (-177 °F) así como con los halógenos, amoníaco y monóxido de carbono. En general, con compuestos orgánicos el cesio experimenta los mismos tipos de reacciones que el resto de los metales alcalinos, pero es mucho más reactivo.
Abundancia
El cesio no es muy abundante en la corteza terrestre, hay solo 7 partes por millón. Al igual que el litio y el rubidio, el cesio se encuentra como un constituyente de minerales complejos, y no en forma de halogenuros relativamente puros, como en el caso del sodio y del potasio. Es hallado frecuentemente en minerales lepidolíticos como los existentes en Rodesia.
Aplicaciones
El cesio metálico se utiliza en celdas fotoeléctricas, instrumentos espectrográficos, contadores de centelleo, bulbos de radio, lámparas militares de señales infrarrojas y varios aparatos ópticos y de detección. Los compuestos de cesio se usan en la producción de vidrio y cerámica, como absorbentes en plantas de purificación de dióxido de carbono, en microquímica. Las sales de cesio se han utilizado en medicina como agentes antishock después de la administración de drogas de arsénico. El isótopo cesio-137 se utiliza habitualmente en procedimientos de radioterapia interna también llamada braquiterapia para el tratamiento del cáncer.
Toxicidad
- Los humanos pueden estar expuestos al cesio por respiración o al ingerirlo con alimentos y bebidas. En el aire los niveles de cesio son generalmente bajos, pero el cesio radioactivo ha sido detectado en algunos niveles en aguas superficiales y en muchos tipos de comidas.
- El cesio está en la naturaleza principalmente a causa de la erosión y desgaste de rocas y minerales. Es también liberado al aire, al agua y al suelo a través de la minería y fábricas de minerales.
- Los isótopos radiactivos del cesio pueden ser disminuidos solo en su concentración a través de la desintegración radiactiva. El cesio no radiactivo puede también ser destruido cuando entra en el ambiente o reacciona con otros compuestos en moléculas muy específicas.
- El cesio en el aire puede viajar largas distancias antes de precipitarse en la tierra. La mayoría de los compuestos del cesio son muy solubles en agua.