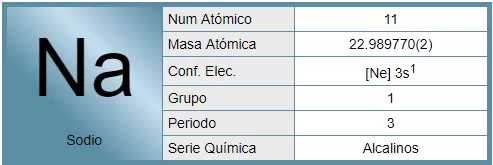
El sodio es un elemento químico de símbolo Na con número atómico 11, es un metal alcalino blando, untuoso, de color plateado, muy abundante en la naturaleza, encontrándose en la sal marina y el mineral halita. Es muy reactivo, arde con llama amarilla, se oxida en presencia de oxígeno y reacciona violentamente con el agua.
El sodio está presente en grandes cantidades en el océano en forma iónica. También es un componente de muchos minerales y un elemento esencial para la vida
Al igual que otros metales alcalinos, el sodio es un metal blando, ligero y de color plateado que no se encuentra libre en la naturaleza. El sodio flota en el agua descomponiéndola, desprendiendo hidrógeno y formando un hidróxido. En las condiciones apropiadas reacciona espontáneamente en el agua.
El sodio metálico se emplea en síntesis orgánica como agente reductor. Es además componente del cloruro de sodio necesario para la vida. Otros usos son:
- En aleaciones antifricción (oro).
- En la fabricación de desodorantes (en combinación con ácidos grasos).
- En la purificación de metales fundidos.
- Se emplea también en la fabricación de células fotoeléctricas.
- Iluminación mediante lámparas de vapor de sodio.
Abundancia
El sodio es relativamente abundante en las estrellas, detectándose su presencia a través de la línea D del espectro solar, situada aproximadamente en el amarillo. La corteza terrestre contiene aproximadamente un 2,6 % de sodio, lo que lo convierte en el sexto elemento más abundante, y el más abundante de los metales alcalinos.
El compuesto más abundante de sodio es el cloruro sódico o sal común, aunque también se encuentra presente en diversos minerales como halita y zeolitas, etc,.
Isótopos
Se conocen trece isótopos de sodio. El único estable es el Na-23. Además existen dos isótopos radioactivos cosmogénicos, Na-22 y Na-24, con períodos de semidesintegración de 2,605 años y aproximadamente 15 horas respectivamente.
Aplicaciones
El sodio metálico se emplea en síntesis orgánica como agente reductor. Es además componente del cloruro de sodio necesario para la vida. Otros usos son:
- En aleaciones antifricción (oro).
- En la fabricación de desodorantes (en combinación con ácidos grasos).
- En la purificación de metales fundidos.
- La aleación Na K, es un material empleado para la transferencia de calor además de desecante para disolventes orgánicos y como reductor. A temperatura ambiente es líquida. El sodio también se emplea como refrigerante.
- Aleado con plomo se emplea en la fabricación de aditivos antidetonantes para las gasolinas.
- Se emplea también en la fabricación de células fotoeléctricas.
- Iluminación mediante lámparas de vapor de sodio.
- Los óxidos Na2O generados por combustión controlada con oxígeno se utilizan para intercambiar el dióxido de carbono por oxígeno y regenerar así el aire en espacios cerrados (p. ej. en submarinos).
- El sodio metálico también se emplea en los laboratorios en la desecación de disolventes.