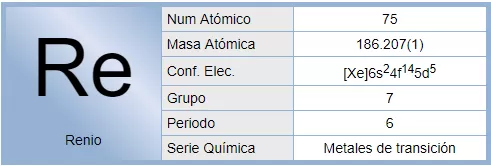
El renio es un elemento químico, de número atómico 75, que se encuentra en el grupo 7 de la tabla periódica de los elementos y cuyo símbolo es Re, descubierto en 1925 por tres científicos alemanes. Es un metal de transición de color blanco-plata, sólido, refractario y resistente a la corrosión, muy utilizado en joyería y como catalizador. Sus propiedades químicas son muy parecidas a las del manganeso, es muy escaso en la corteza terrestre y se obtiene principalmente a partir de minerales de molibdeno.
Existen 35 isótopos y 26 radioisótopos de este elemento, de los cuales los más estables son el 185Re y el 187Re. Los principales yacimientos de renio se encuentran en América y Asia, destacando los de Chile y Kazajistán.
Abundancia
Los países con mayor producción de renio son Chile y Kazajistán, con 22 900 y 8000 toneladas respectivamente, extraídas en 2007. Otros países involucrados en la producción de renio son Estados Unidos, Armenia, Canadá, Perú y Rusia. La suma de extracciones de renio entre estos siete países es superior a 49 000 toneladas, cantidad que ha aumentado de 2006 a 2007 con una diferencia de más de 2000 kilogramos.
Existen dos métodos de obtención de renio. El primero sería mediante el procesado del molibdeno, que una vez extraído debe ser tratado con ácido nítrico o sulfúrico. La segunda manera es la reducción de perrenato amónico (NH4ReO4) con hidrógeno a una temperatura muy alta. También se puede obtener óxido de renio mediante el tratamiento de algunas sustancias generadas en la tostación de molibdenita, que se reducen con hidrógeno obteniéndose el compuesto en forma de polvo. Es uno de los elementos más escasos en la corteza terrestre, concretamente el número 79 en abundancia.
Isótopos
Se han descubierto un total de 35 isótopos de renio. En la naturaleza existen dos isótopos estables, 185Re y 187Re, de los cuales el 187Re es el más abundante —62,6% de abundancia natural— y tiene una vida media de 4,35 x 1010 años. Este tiempo de vida se ve afectado en gran parte por la carga de sus átomos. La desintegración beta de los 187Re se utiliza para la datación de minerales de este elemento y de osmio, cuya energía disponible para este decaimiento es de 2,6 ev, una de las energías más bajas conocidas entre todos los radionucleidos. En medicina, son muy utilizados los radioisótopos 186Re y 188Re que tienen una vida media muy corta. En total, hay 26 radioisótopos.
Aplicaciones
El renio, al ser un elemento metálico refractario y resistente a la corrosión, es usado principalmente en joyería, en la construcción de filamentos para espectrómetros de masas y como catalizador de reacciones de hidrogenación y deshidrogenación en la industria química. En menor escala se utiliza en aleaciones de wolframio y molibdeno, como conductor eléctrico, en la fabricación de flashes fotográficos y para la construcción de los plumines de las estilográficas. Recientemente científicos chilenos han desarrollado un compuesto derivado del renio que ataca a las células cancerosas, pasando a ser utilizado en medicina para el diagnóstico y tratamiento del cáncer.
Precauciones
Se sabe muy poco acerca de la toxicidad que pueden tener el renio y sus compuestos, ya que estos se utilizan en cantidades muy pequeñas. Las sales solubles que contienen este elemento, como perrenatos y haluros, sí pueden ser peligrosas. Se ha demostrado que algunos de estos compuestos tienen una toxicidad aguda en ratas. Los perrenatos de renio tienen DL50 de 2800 mg/kg —una toxicidad bastante baja— mientras que el tricloruro de renio mostró DL50 de 280 mg/kg, una toxicidad diez veces mayor. En algunos casos, al ser un elemento radionucleido, manifiesta radiación de partículas alfa y rayos X.
Sus efectos en animales engloban irritación en ojos, piel e incluso en vías respiratorias en caso de inhalación, provocando fibrosis pulmonar y mareos en caso de recibir el contacto de un vapor derivado de este elemento. El impacto ambiental del renio se reduce a la expulsión de gases tóxicos en la industria una vez utilizado. Los compuestos de renio más peligrosos son el ReS7, que se inflama al contactar con el aire