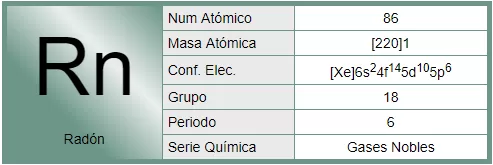
El radón es un elemento químico perteneciente al grupo de los gases nobles. En su forma gaseosa es incoloro, inodoro e insípido y en forma sólida su color es rojizo. En la tabla periódica tiene el número 86 y símbolo Rn. Su masa media es de 222, lo que implica que por término medio tiene 222-86 = 136 neutrones. Igualmente, en estado neutro le corresponde tener el mismo número de electrones que de protones, esto es, 86.
Es un elemento radiactivo y gaseoso, encuadrado dentro de los llamados gases nobles.
El radón es producto de la desintegración del radio (226Ra), elemento altamente radiactivo. El isótopo 219Rn es producto de la desintegración del actinio, llamado actinón y tiene una vida media de 4 segundos. Además de todos estos, el radón tiene 22 isótopos artificiales, producidos por reacciones nucleares por transmutación artificial en ciclotrones y aceleradores lineales. El isótopo más estable es el 222Rn, también el más abundante, con una vida media de 3,8 días y producto de la desintegración del 226Ra. Al emitir partículas alfa se convierte en 218Po.
Aplicaciones
La emanación del radón del suelo varía con el tipo de suelo y con el contenido de uranio superficial, así que las concentraciones al aire libre del radón se pueden utilizar para seguir masas de aire en un grado limitado. Este hecho ha sido puesto al uso por algunos científicos atmosféricos.
Aunque algunos médicos creyeron una vez que el radón se puede utilizar terapéuticamente, no hay evidencia para esta creencia y el radón no está actualmente en uso médico, por lo menos en el mundo desarrollado.
Precauciones
Cuando se habla del peligro del radón no se debe olvidar la radiación emitida por todo el conjunto: radón y descendientes. El peligro está sobre todo en sus descendientes de vida corta: en concreto el 218Po y 214Po. Existe también una exposición externa causada por la radiación gamma directa, pero el verdadero riesgo está en las partículas alfa.
La radiación alfa es relativamente poco peligrosa fuera del cuerpo porque la epidermis nos protege de ella. El principal problema viene cuando se inhala: las partículas radioactivas se adhieren al tejido pulmonar, donde pueden emitir radiación alfa a las células broncopulmonares. La absorción de esta radiación provoca ionizaciones y excitaciones de las estructuras celulares provocando efectos lesivos: puede dañar directa e indirectamente el DNA y provocar mutaciones en el tejido pulmonar. Recordemos que el cáncer es una división incontrolada de células mutadas. En EE. UU. está considerada la segunda causa de muerte por cáncer de pulmón después del tabaco. Además, sus efectos son sinérgicos: fumar y vivir en una casa con alto contenido de radón aumenta el riesgo unas 46 veces más que de darse los 2 fenómenos por separado.
Un estudio en Alemania nos dice que con una concentración de 40 Bq/m3 el 7% de todos los cánceres de pulmón en fumadores se puede atribuir al radón. En no fumadores se puede atribuir hasta un 22%. Esto es lógico porque en fumadores es difícil atribuir una sola causa. Otros estudios en no fumadores en Francia nos dicen que puede llegar a atribuirse hasta un 25%. En Holanda un 17% y en Suecia un 24%. En Galicia la combinación de Tabaco y radón se atribuye en un 25%. La recomendación de protección radiológica en Europa establece el nivel de referencia acción de remedio 400 Bq/m3. Y el nivel de diseño de nuevas viviendas en 200 Bq/m3. La agencia norteamericana de protección ambiental establece como el nivel de acción cuando se superan los 4 PCi/l (148 Bq/m3).